آنزیم
آنزیم یک نوع «کاتالیست» (catalyst) بیولوژیکی است که سرعت واکنش شیمیایی را در موجود زنده تنظیم میکند. اکثر آنزیمها پروتئینها هستند؛ اگرچه برخی نوکلئیک اسیدها به نام ریبوزومها هم قادر به انجام فعالیت کاتالیز محسوب میگردند.
آنزیمها برای حفظ حیات ضروری هستند؛ زیرا اکثر واکنشهای شیمیایی در سلولهای بیولوژیکی مانند هضم غذا، خیلی آرام اتفاق میافتند یا منجر به محصولات مختلفی بدون فعالیت آنزیمها میگردند. اکثر بیماریهای ارثی نتیجهی یک جهش ژنتیکی، تولید بیش از حد یا کمبود یک آنزیم حساس هستند. برای مثال، «عدم تحمل لاکتوز یا نارسایی لاکتاز» (lactose intolerance) که به معنای عدم توانایی هضم مقادیر قابل توجه لاکتوز که قند اصلی در شیر است، ناشی از کمبود آنزیم لاکتاز است.
یک آنزیم برای اینکه کاربردی باشد، باید به یک شکل سه بعدی دقیق تبدیل گردد. این که چطور چنین ساختار پیچیدهای شکل میگیرد، هنوز به شکل راز باقی مانده است. یک زنجیرهی کوچک از 150 آمینواسید یک آنزیم را شکل میدهد که تعداد بسیار زیادی پیکربندی مختلف دارد: اگر 1012 پیکربندی مختلف در هر ثانیه آزمایش گردند، حدود 1026 سال برای یافتن و درک یک مدل زمان مورد نیاز است.
با این حال یک آنزیم «دناتوره شده یا واسرشته» (denatured) میتواند در کسری از ثانیه تغییر شکل و سپس به طور دقیق در یک واکنش شیمیایی واکنش نشان دهد. برخی دانشمندان تصور میکنند، اثرات «کوانتومی» (quantum) حتی در فواصل بزرگ (با استانداردهای اتمی) که توسط یک مولکول پروتئین ظهور میکند، منجر به ایجاد رفتارهای اینچنینی میگردد. این آنزیمها نوعی پیچیدگی مبهوتکننده و توازن یا هارمونی را در جهان اثبات میکنند.
در حالی که تمام آنزیمها نقش بیولوژیکی دارند، بعضی از آنها به صورت تجاری مورد استفاده قرار میگیرند. به عنوان مثال، بسیاری از پاککنندههای خانگی از آنزیمها برای افزایش سرعت تجزیهی لکههای پروتئین یا نشاسته روی لباسها استفاده میکنند.
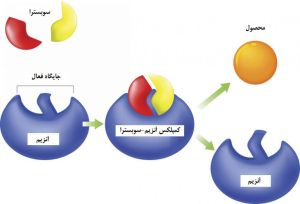
مانند تمام کاتالیستها، آنزیمها هم برای کاهش انرژی فعالسازی یک واکنش یا انرژی ابتدایی لازم برای رخ دادن اکثر واکنشهای شیمیایی به کار میروند. گرما را نمیتوان به یک سیستم زنده اضافه کرد، بنابراین آنزیمها یک مسیر جایگزین را فراهم میکنند: آنها با یک زیرلایه (مواد موجود در واکنش شیمیایی) برای تشکیل یک «حالت گذار» (transition state)، یک «کمپلکس واسطهی ناپایدار» (unstable intermediate complex) که نیاز به انرژی کمتری برای پیشروی واکنش دارد، پیوند میدهند.
همانند یک کاتالیست، آنزیم طی واکنش تکمیل شده بدون تغییر باقی میماند؛ بنابراین میتواند به فعل و انفعال با زیرلایهها ادامه دهد. آنزیمها ممکن است طی فرایندی به خصوص سرعت واکنشها را تا چندین میلیون برابر افزایش دهند. آنزیمها میتوانند توسط مولکولهایی که فعالیت آن را افزایش میدهد، «راهانداز» (activator)، یا مولکولهایی که باعث کاهش فعالیت آنها میگردد، «مهارکننده» (inhibitor) تحت تاثیر قرار گیرند. بسیاری از داروها با مهار آنزیمها در بدن عمل میکنند و اثر خود را نشان میدهند. «آسپیرین» (aspirin) از طریق مهار آنزیمهای «COX-1» و «COX-2» کار میکند. آنزیمهایی که «پروستاگلاندین» (prostaglandin) تولید میکنند، یک پیامرسان هورمونی برای نشان دادن التهاب به شمار میروند. با مهار فعالیت این آنزیمها، «آسپیرین» (aspirin) تجربهی ما از درد و التهاب را سرکوب میکند.
ساختار
ساختار آنزیم مهم است، زیرا عملکرد خاص آنزیم در بدن را تعیین میکند. آنزیمها (و سایر پروتئینها) از زنجیرههای اسید آمینه به نام زنجیرههای «پلیپپتیدی» (polypeptide) تشکیل شدهاند. دنبالهی خطی آمینواسیدها تعیینکنندهی مشخصات تاشدگی زنجیرهها به یک ساختار سه بعدی است. یک آنزیم ممکن است فقط یک زنجیرهی پلیپپتیدی داشته باشد که معمولا یک صد آمینواسید یا تعداد بیشتری را به هم پیوند میدهد یا ممکن است شامل چندین زنجیرهی پلیپپتیدی باشد که با هم به عنوان یک واحد عمل میکنند. اکثر آنزیمها بزرگتر از زیرلایههایی هستند که روی آن عمل میکنند. فقط یک قسمت خیلی کوچک از آنزیم، تقریبا 10 آمینواسید، دارای تماس مستقیم با زیرلایهها است. این ناحیه، جایی که پیوند بین زیرلایهها و واکنش اتفاق میافتد، به عنوان سایت فعال آنزیم شناخته میشود.